醫(yī)藥行業(yè)微利時(shí)代正式啟幕!中小企業(yè)如何留在“賽場(chǎng)”
日期:2017/2/23

國(guó)務(wù)院辦公廳2月9日發(fā)布的《關(guān)于進(jìn)一步改革完善藥品生產(chǎn)流通使用政策的若干意見(jiàn)》(以下簡(jiǎn)稱(chēng)“若干意見(jiàn)”),是從全產(chǎn)業(yè)鏈角度發(fā)布的政策,對(duì)醫(yī)藥行業(yè)上下游合規(guī)的指導(dǎo)意義明確。在生產(chǎn)流通使用環(huán)節(jié)的嚴(yán)格控制下,利潤(rùn)分配格局基本已定,微利時(shí)代正式來(lái)臨。
醫(yī)藥行業(yè)曾經(jīng)所擁有人口紅利、制度紅利、WTO紅利、市場(chǎng)紅利、資源和產(chǎn)能紅利、金融和貿(mào)易紅利等增長(zhǎng)利好因素,在醫(yī)保基金承壓下,這些紅利已經(jīng)基本到底。
科技和信息化紅利將是未來(lái)我國(guó)醫(yī)藥行業(yè)的增長(zhǎng)點(diǎn)。然而,信息扁平化的背景下,企業(yè)競(jìng)爭(zhēng)加劇,我國(guó)醫(yī)藥行業(yè)的洗牌在短期內(nèi)仍會(huì)進(jìn)行,長(zhǎng)期利好“優(yōu)勝劣汰”后剩下來(lái)的企業(yè)。
價(jià)格透明,利潤(rùn)分配決定項(xiàng)目偏好
“若干意見(jiàn)”中提到的藥品價(jià)格有藥品出廠(口岸)價(jià)格、藥品招標(biāo)采購(gòu)價(jià)格、藥品醫(yī)保判價(jià)格、醫(yī)保支付/結(jié)算價(jià)格等。隨著“兩票制”的推開(kāi),食品藥品監(jiān)管、衛(wèi)生計(jì)生、人力資源社會(huì)保障、價(jià)格、稅務(wù)、工商管理、公安等部門(mén)嚴(yán)厲打擊價(jià)格欺詐和價(jià)格壟斷等違法違規(guī)行為,加之藥品價(jià)格監(jiān)測(cè)體系的健全、藥品出廠價(jià)格信息可追溯機(jī)制的建立,以及對(duì)原產(chǎn)國(guó)或我國(guó)周邊價(jià)格的采集等“組合拳”,藥品各環(huán)節(jié)的價(jià)格信息基本透明。增值稅的流轉(zhuǎn)稅特征也讓利潤(rùn)信息越來(lái)越透明。
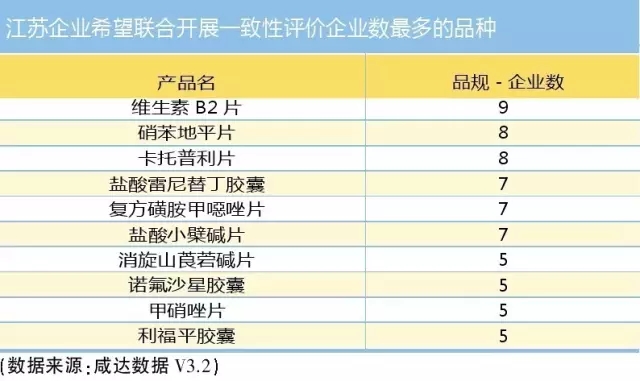
價(jià)格與利潤(rùn)基本確定之下,市場(chǎng)趨利本性促使企業(yè)選擇產(chǎn)品立項(xiàng)會(huì)更關(guān)注市場(chǎng)潛力。而研發(fā)成本與費(fèi)用、項(xiàng)目成功率和風(fēng)險(xiǎn)也同樣信息透明。假設(shè)一個(gè)仿制藥項(xiàng)目獲得生產(chǎn)批件之前企業(yè)的投入為1000萬(wàn)元,未來(lái)競(jìng)爭(zhēng)廠家有5~10家,考慮到后續(xù)品牌的市場(chǎng)投入以及藥品生產(chǎn)周期,生產(chǎn)廠家會(huì)傾向于選擇終端銷(xiāo)售規(guī)模潛力過(guò)億的項(xiàng)目。對(duì)于銷(xiāo)售量較大但價(jià)格較低的普藥,更多企業(yè)會(huì)選擇“聯(lián)合抱團(tuán)”,這從江蘇所公布企業(yè)希望聯(lián)合開(kāi)展一致性評(píng)價(jià)品種表也可以看出,銷(xiāo)售量較大的維生素B2片、硝苯地平片和卡托普利片等基藥產(chǎn)品企業(yè)更希望能夠抱團(tuán)。
2015年以化合物/有效成分統(tǒng)計(jì),樣本醫(yī)院過(guò)億元市場(chǎng)規(guī)模的產(chǎn)品共有342個(gè),這342個(gè)產(chǎn)品中還包括在合理用藥大潮下用量面臨萎縮的輔助用藥和營(yíng)養(yǎng)用藥等產(chǎn)品。“若干意見(jiàn)”將會(huì)推動(dòng)終端銷(xiāo)售用量信息更加透明化,這意味著一方面輔助用藥和營(yíng)養(yǎng)用藥等產(chǎn)品的用量會(huì)被嚴(yán)格限制未來(lái)有可能會(huì)踢出過(guò)億元清單;另一方面過(guò)億元的產(chǎn)品清單是各仿制藥生產(chǎn)廠家必爭(zhēng)之品種,競(jìng)爭(zhēng)會(huì)更激烈。
研究注冊(cè)信息會(huì)發(fā)現(xiàn),大多數(shù)過(guò)億的項(xiàng)目已被正大天晴、恒瑞、豪森、齊魯、石藥等企業(yè)在研發(fā)項(xiàng)目未提價(jià)之前“買(mǎi)買(mǎi)買(mǎi)”提前布局,中小企業(yè)想要現(xiàn)在才進(jìn)場(chǎng)參與仿制競(jìng)賽,將要花費(fèi)5倍~10倍的成本。
中小企業(yè)的資金限制,導(dǎo)致其一年最多投入3個(gè)項(xiàng)目。中小企業(yè)選擇項(xiàng)目方向有三:
一是根據(jù)自身企業(yè)的銷(xiāo)售強(qiáng)勢(shì)領(lǐng)域選擇銷(xiāo)售規(guī)模前列、競(jìng)爭(zhēng)較大的項(xiàng)目拼一致性評(píng)價(jià)排名前五甚至前三的位置。
二是規(guī)避大公司選擇的熱門(mén)領(lǐng)域,選擇競(jìng)爭(zhēng)較少且產(chǎn)品周期相對(duì)久一點(diǎn)的細(xì)分小領(lǐng)域項(xiàng)目,如罕見(jiàn)病。
三是選擇免臨床、成本低的項(xiàng)目,制劑方面如注射劑、滴眼劑,治療領(lǐng)域如兒童藥和中藥經(jīng)方等。值得注意的是,此類(lèi)產(chǎn)品未必大企業(yè)不會(huì)布局,恒瑞系滴眼液的生產(chǎn)批文8個(gè),包括拉坦前列素滴眼液、馬來(lái)酸噻嗎洛爾滴眼液、鹽酸洛美沙星滴眼液、鹽酸羥甲唑啉滴眼液、萘敏維滴眼液、妥布霉素滴眼液和妥布霉素地塞米松滴眼液7個(gè)通用名產(chǎn)品。在申報(bào)生產(chǎn)/已獲臨床批件的產(chǎn)品3個(gè),分別是瑞巴派特滴眼液、苯磺貝他斯汀滴眼液和貝美前列素滴眼液。
產(chǎn)品線開(kāi)始出現(xiàn)斷層
生產(chǎn)企業(yè)在中短期內(nèi)承受?chē)?guó)家“提高醫(yī)藥產(chǎn)業(yè)集中度”相關(guān)政策嚴(yán)控的壓力越來(lái)越大,短期要面臨的政策主要涉及“原輔料變更、生產(chǎn)工藝調(diào)整”生產(chǎn)方面的檢查,中長(zhǎng)期所要面臨的市場(chǎng)壓力涉及臨床路徑管理政策的落地、醫(yī)藥代表學(xué)術(shù)推廣行為嚴(yán)控等關(guān)于合理用藥方面的限制,個(gè)別產(chǎn)品還要面臨“兩票制”“醫(yī)藥分開(kāi)”后渠道市場(chǎng)壓縮的困境,以上政策將加快推動(dòng)已上市產(chǎn)品的市場(chǎng)結(jié)構(gòu)變化。
新藥要求滿(mǎn)足臨床需求,仿制藥需要過(guò)一致性評(píng)價(jià),臨床試驗(yàn)數(shù)據(jù)核查從嚴(yán),國(guó)內(nèi)的藥品批文獲批的門(mén)檻在提升。“若干意見(jiàn)”推進(jìn)之下,預(yù)計(jì)我國(guó)上市的產(chǎn)品通用名、藥品批文、生產(chǎn)廠家整體數(shù)量將會(huì)持續(xù)減少,其中輔助用藥、營(yíng)養(yǎng)類(lèi)藥品等批文將是短期影響較大的產(chǎn)品。大批量生產(chǎn)廠家手中的產(chǎn)品批文要作廢,新批文又拿不到,產(chǎn)品線出現(xiàn)斷層,被迫退出市場(chǎng)。最終達(dá)成“推動(dòng)落后企業(yè)退出,著力化解藥品生產(chǎn)企業(yè)數(shù)量多、規(guī)模小、水平低等問(wèn)題”的目標(biāo)。
“若干意見(jiàn)”中短期利好已提前布局產(chǎn)品管線且項(xiàng)目質(zhì)量靠譜的企業(yè),特別是在美國(guó)已成功上市仿制藥產(chǎn)品的企業(yè),如恒瑞、華海、石藥和華潤(rùn)等。
產(chǎn)品結(jié)構(gòu)調(diào)整對(duì)主營(yíng)收入為抗生素、輔助用藥和營(yíng)養(yǎng)類(lèi)藥品的生產(chǎn)企業(yè)及其下游代理商影響最大。短期內(nèi)此類(lèi)生產(chǎn)企業(yè)面臨生存壓力最大,尋求轉(zhuǎn)型的渴望是最為迫切的。項(xiàng)目費(fèi)用決定了企業(yè)不能像以往那樣簡(jiǎn)單重復(fù)地立項(xiàng),信息獲取、信息整合在立項(xiàng)中的作用越來(lái)越重要。
項(xiàng)目費(fèi)用居高不下將導(dǎo)致銷(xiāo)售規(guī)模有限的低價(jià)藥無(wú)廠家有動(dòng)力去開(kāi)展一致性評(píng)價(jià)項(xiàng)目,此類(lèi)產(chǎn)品未來(lái)更多可能是國(guó)企定點(diǎn)生產(chǎn)、定點(diǎn)供給。
“兩票制”的執(zhí)行除了推高流通行業(yè)集中度的上升幅度,還會(huì)導(dǎo)致行業(yè)的流通層級(jí)的扁平化。“醫(yī)藥分開(kāi)”更多的是渠道分流的工作,社會(huì)藥店分擔(dān)原來(lái)醫(yī)院門(mén)診藥房所承擔(dān)的工作。“若干意見(jiàn)”鼓勵(lì)藥品流通往下游整合,從而形成藥品流通企業(yè)批發(fā)零售一體化經(jīng)營(yíng),這意味著我國(guó)未來(lái)終端的競(jìng)爭(zhēng)模式主要是幾家大流通企業(yè)在整合大型連鎖零售藥房后形成“巨無(wú)霸”企業(yè)(如華潤(rùn)、國(guó)藥、上藥)之間的寡頭競(jìng)爭(zhēng)態(tài)勢(shì)。
臨床醫(yī)療機(jī)構(gòu)方面,醫(yī)院臨床用藥目錄若是參考安徽、福建省,先從臨床需求確定各學(xué)科必需用藥目錄再整合成一個(gè)省專(zhuān)用的醫(yī)院采購(gòu)目錄,并且隨著臨床路徑的推進(jìn)基本固化各醫(yī)院藥品用藥目錄,最終全國(guó)的醫(yī)療機(jī)構(gòu)臨床用藥目錄內(nèi)藥品結(jié)構(gòu)重合比例有望高達(dá)70%以上,而不會(huì)像現(xiàn)在那樣,各醫(yī)院臨床用藥目錄間差距較大。藥品對(duì)醫(yī)療機(jī)構(gòu)的市場(chǎng)準(zhǔn)入,未來(lái)基本上拼的就是臨床證據(jù)。
流通行業(yè)的變革過(guò)程也是我國(guó)醫(yī)藥行業(yè)藥品結(jié)構(gòu)變革的過(guò)程。藥品企業(yè)和流通使用環(huán)節(jié)都強(qiáng)勢(shì)的情況下,短期生產(chǎn)環(huán)節(jié)和流通環(huán)節(jié)兩大頭將會(huì)要求中間環(huán)節(jié)利潤(rùn)壓縮,代理、醫(yī)藥代表及醫(yī)生處方提成將面臨費(fèi)用縮減。長(zhǎng)期而言,大商業(yè)寡頭企業(yè)會(huì)從產(chǎn)品發(fā)展周期出發(fā),控制仿制藥的準(zhǔn)入廠家數(shù)以保證利潤(rùn),中小型仿制藥生產(chǎn)企業(yè)會(huì)傾向于選擇一家大商業(yè)寡頭形成緊密合作關(guān)系以保證銷(xiāo)售渠道的覆蓋。
未來(lái)紅利的思考
社交媒體推薦藥品使用,電子支付在醫(yī)療機(jī)構(gòu)的普遍覆蓋等,科技和信息化紅利將是未來(lái)我國(guó)醫(yī)藥行業(yè)的增長(zhǎng)點(diǎn)。
但信息科技將會(huì)如何顛覆醫(yī)藥行業(yè)的效應(yīng)暫時(shí)還未能體現(xiàn)。發(fā)改委2016年版《戰(zhàn)略性新興產(chǎn)業(yè)重點(diǎn)產(chǎn)品和服務(wù)指導(dǎo)目錄》所提到的“數(shù)據(jù)制藥”“人工智能系統(tǒng)”也沒(méi)有在“若干意見(jiàn)”中得到體現(xiàn)。
此外,上市許可持有人制度短期而言主要用于代工生產(chǎn),對(duì)研發(fā)機(jī)構(gòu)的激勵(lì)效應(yīng)還需要長(zhǎng)遠(yuǎn)觀察。上市許可持有人制度長(zhǎng)期會(huì)激勵(lì)醫(yī)藥行業(yè)分工細(xì)化,若國(guó)家的重大新藥創(chuàng)制科技重大專(zhuān)項(xiàng)等國(guó)家科技計(jì)劃(專(zhuān)項(xiàng)、基金等)配套到位,擁有前沿科技以科學(xué)家為主導(dǎo)的微小科研機(jī)構(gòu)將興起。
信息來(lái)源:醫(yī)藥經(jīng)濟(jì)報(bào)
|